 2021.06.11
2021.06.11  1914次
1914次

前言
帕金森病(PD)是最普遍的神经退行性疾病之一,影响2%-3%的65岁及以上人群。一般来说,PD的特征是中脑黑质中多巴胺能神经元的选择性缺失。研究人员已经报道了PD的多种分子机制,如线粒体功能障碍、氧化应激、轴突运输、Ca2+稳态和神经炎症。特别是,α-synuclein (α-Syn) (路易体的胞内成分)被认为是PD最重要的神经病理学特征之一。在PD患者的多巴胺能神经元、MPTP(四氢吡啶)处理的动物和MPP+(MPTP代谢物)处理的神经母细胞瘤细胞中观察到α-Syn的积累。此外,有研究报道,α-Syn突变(A30P、A53T和E46K)是罕见家族性PD的主要原因。
因此,清除α-Syn为帕金森病的治疗提供了一种合理的途径。自噬被认为在降解细胞内α-Syn聚集物中起着重要作用。Rapamycin(雷帕霉素)已被证明通过诱导自噬减少α-Syn聚集,从而在体内和体外保护多巴胺能神经元抵抗死亡。不幸的是,Rapamycin缺乏特异性,常常导致口腔和呼吸道感染、白细胞减少、口腔炎、高胆固醇血症、高甘油三酯血症、免疫抑制等多种副作用,从而限制了Rapamycin在PD治疗中的应用。因此,目前迫切需要寻找其他能够清除α-Syn聚集物但副作用更少的PD候选治疗方法。
GM1神经节苷脂(18:1/18:0)是一种主要的脑神经节苷脂,由三个结构单元组成:一个低聚糖,一个神经酰胺锚点和几个唾液酸残基。由于其对神经元可塑性、神经营养物质的释放、神经传递以及与神经调节蛋白的相互作用的调节作用,这种分子被认为是各种大脑功能中必不可少的调节剂。外源性神经节苷脂已经被证明可以影响中枢神经系统中的多巴胺能、谷氨酸能和胆碱能神经元的存活。GM1神经节苷脂的治疗作用已在PD患者,以及MPTP治疗的小鼠和灵长类动物,显示神经保护或神经修复作用。尽管有这些积极的数据,但GM1神经节苷脂治疗PD的确切机制仍不确定。在以前的报道中,这种治疗方法被猜测以自噬依赖的方式降解α-Syn,这促使作者研究自噬是否参与GM1神经节苷脂的抗PD机制。
研究结果
1. GM1神经节苷脂改善了C57BL/6 J小鼠MPTP诱导的行为缺陷,并恢复了多巴胺及其代谢产物的水平
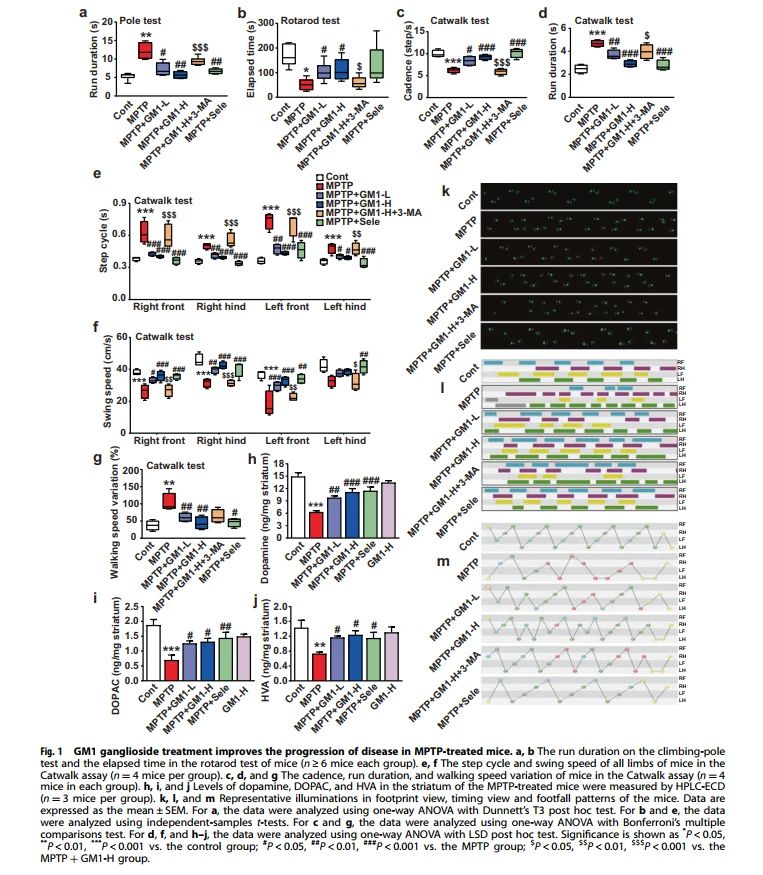
MPTP被酶MAO-B转化为毒性代谢物MPP+,通过抑制线粒体电子传递链复合物I杀死多巴胺能神经元。因此,MPTP和MPP+通常分别在体内和体外诱导一种与PD相似的神经元细胞毒性综合征。在本研究中,C57BL/6 J小鼠腹腔注射MPTP (30 mg/kg) 5天建立PD模型,以评估GM1神经节苷脂的保护作用。治疗2周后,进行行为测试,包括爬杆测试、旋转测试和步态分析。如(图1a)所示,MPTP处理的小鼠比对照组小鼠花更多的时间爬杆。相比之下,GM1神经节苷脂(静脉注射,25和50 mg/k)和selegiline(司来吉林MAO-B抑制剂,静脉注射,60 mg/kg)显著减少MPTP治疗的小鼠爬杆时间。在旋转测试中,MPTP处理显著降低了下降潜伏期,为MPTP所致的运动功能障碍。GM1神经节苷脂和selegiline可抑制MPTP诱导的下降潜伏期的下降(图1b)。
作者进一步评估了GM1神经节苷脂对步态的治疗作用,通过包括步速、摆动速度、步频、跑步持续时间和步行速度等参数的猫步试验。如(图1c-g)所示,MPTP处理小鼠的摆动速度和步频显著下降,而在步数周期、跑步持续时间和步行速度上,则观察到显著增加。相比而言,GM1神经节苷和selegiline的治疗有效改善了MPTP引起的这些步态行为障碍(图1c-g)。此外,GM1神经节苷治疗恢复了步态表现(图1k)。在MPTP处理的小鼠中,增加了四肢的触摸和悬挂次数(图1l),和步法模式的数量(图1m)。这些行为测试提示GM1神经节苷脂对PD有明显的治疗作用。值得注意的是,GM1神经节苷脂在三个行为测试中的保护作用被3-MA(自噬抑制剂)逆转(图1 a-g和k-m)。这一发现表明,GM1神经节苷脂的保护作用可能与自噬有关。
此外,采用高效液相色谱-电化学检测小鼠纹状体中多巴胺及其代谢产物的水平。如(图1h-j)所示,MPTP处理显著降低了多巴胺、二羟基苯乙酸(DOPAC)和高香草酸(HVA)的水平。GM1神经节苷脂和selegiline治疗可防止MPTP诱导的多巴胺、DOPAC和HVA水平减少,提示GM1神经节苷脂能有效改善多巴胺能神经元的功能。
2. GM1神经节苷脂改善MPP+诱导的神经毒性,减少神经元细胞中α-Syn的积累
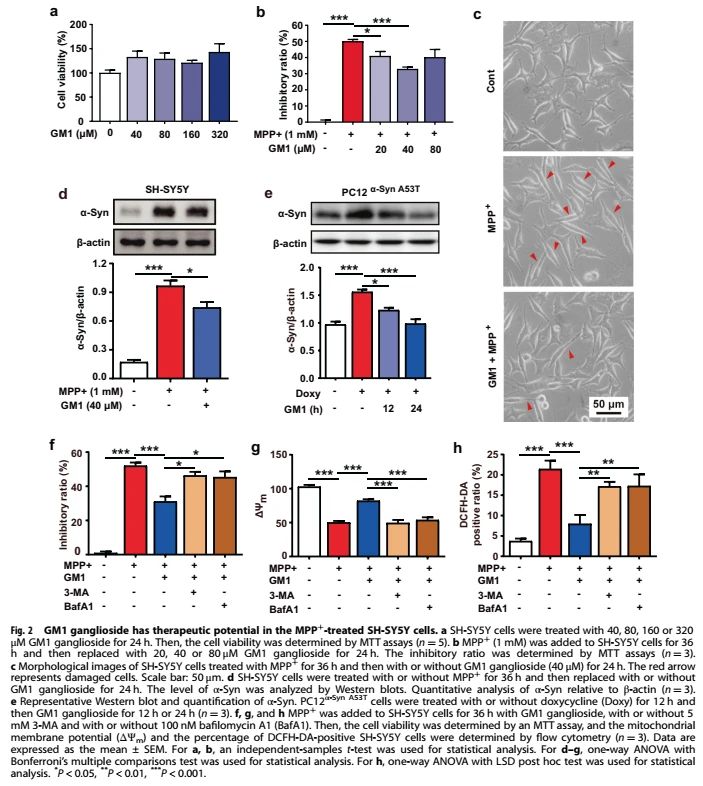
MPTP的代谢物MPP+在体外可导致神经毒性。因此,作者进一步利用MPP+验证GM1神经节苷脂对SH-SY5Y细胞的神经保护作用。如(图2a)所示,GM1神经节苷脂浓度小于320μM时不引起任何细胞毒性。MPP+ (1 mM)显著抑制细胞增殖,而不同浓度的GM1神经节苷脂(20、40和80 μM)处理可显著减弱MPP+诱导的细胞增殖抑制(图2b)。此外,MPP+导致细胞形态发生明显变化,伪足减少,胞体拉长,GM1神经节苷脂使其恢复(图2c)。Western blot分析显示,GM1神经节苷脂处理显著抑制MPP+诱导的SH-SY5Y细胞钟α-Syn积累(图2d)。同样,GM1神经节苷脂以时间依赖性的方式降低了PC12α-Syn A53T细胞中的α-Syn过表达作用(图2e)。
线粒体功能缺陷和氧化应激已在PD的发病机制中得到证实。如(图2g和h)所示,1 mM MPP+处理SH-SY5Y细胞36 h后,线粒体膜电位(δ ψ m)明显降低,ROS水平升高,而GM1神经节苷脂治疗明显抑制了这些变化。此外,自噬抑制剂(3-MA或bafilomycin A1)可消除GM1神经节苷脂的治疗效果。这些体外研究结果与MPTP处理的小鼠的观察结果一致,进一步提示自噬激活参与了GM1神经节苷脂对PD的保护作用。
3. GM1神经节苷脂诱导神经元细胞自噬
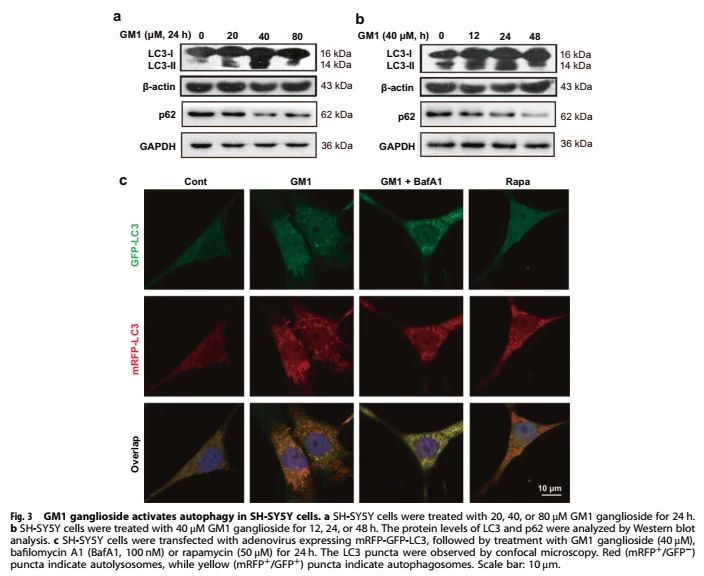
已有研究报道GM1神经节苷脂可诱导促进多种细胞系自噬。体外实验显示,不同剂量的GM1神经节苷脂处理SH-SY5Y细胞后,自噬标记物LC3-II增加和自噬底物SQSTM1/p62的降解均增强,特别是在40 μM(图3a)。另外,在该剂量下,GM1神经节苷脂对细胞处理24 h后,这些自噬相关蛋白的影响最为明显(图3b)。为更直观的观察GM1神经节苷脂对细胞自噬的促进作用,作者使用mRFP-GFP-LC3标记进行自噬通量测定。Rapamycin(雷帕霉素)通过抑制mTOR[45]发挥自噬诱导作用,作为阳性对照。由于GFP对低pH条件敏感,当自噬小体与溶酶体融合时,GFP(绿色)荧光被熄灭,只能观察到mRF(红色)荧光。当GFP和mRFP(黄色)荧光同时出现时,说明自噬小体不与溶酶体结合。与对照组相比,GM1神经节苷脂和Rapamycin处理的细胞中红色斑点明显增多,而GM1神经节苷脂和bafilomycin A1联合处理可增强黄色斑点(图3c),说明GM1神经节苷脂增强了SHSY5Y细胞的自噬通量。
4. GM1神经节苷脂激活自噬有助于清除α-Syn
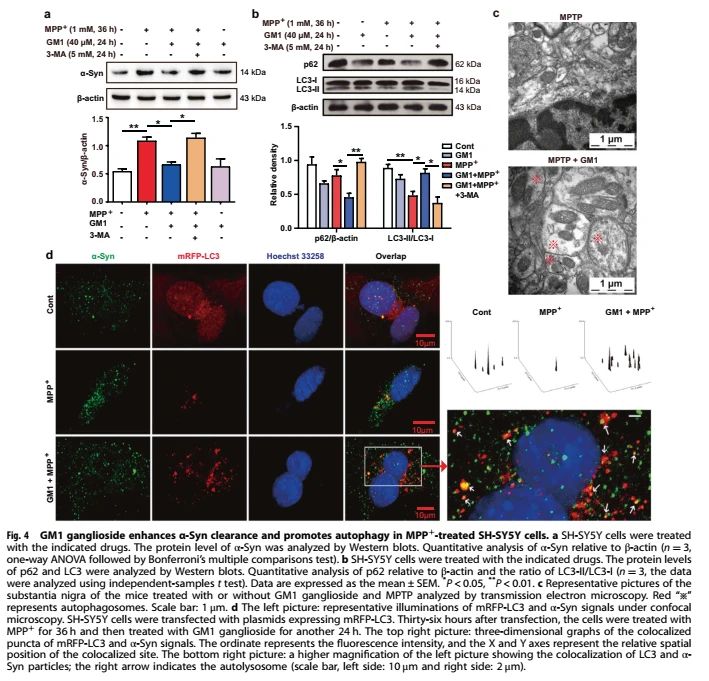
由于去除异常的α-Syn为PD的治疗提供了一个很有潜力的策略,早期研究表明自噬介导的α-Syn降解有利于对PD的保护作用。GM1神经节苷脂对MPTP诱导的小鼠及MPP+诱导的细胞的保护作用被3-MA和bafilomycin A1阻断,说明可能与自噬激活有关。如预期的那样,3-MA显著消除了GM1神经节苷脂对MPP+处理SH-SY5Y细胞中α-Syn蛋白水平的影响(图4a)。作者随后进一步确定GM1神经节苷脂对自噬过程的影响。数据显示,MPP+存在下,GM1神经节苷脂处理明显促进了SH-SY5Y细胞中LC3-I向LC3-II的转化,同时自噬底物SQSTM1/p62蛋白水平下降(图4b)。此外,透射电镜显示,GM1神经节苷脂处理小鼠的黑质中存在明显的自噬泡(图4c)。重要的是,共聚焦显微镜图像显示GM1神经节苷脂诱导的自噬小体与MPP+诱导的α-Syn共定位(图4d)。这些体内和体外数据表明,GM1神经节苷脂激活自噬,参与α-Syn清除。
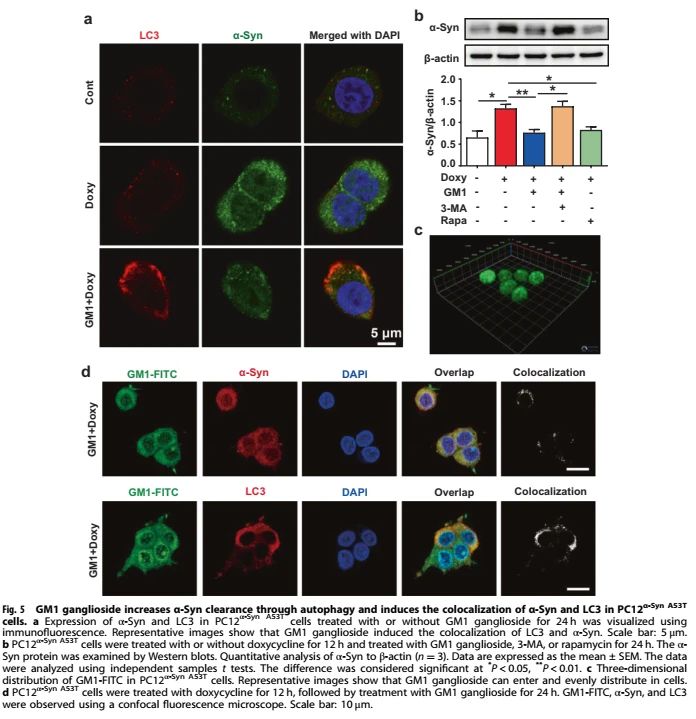
此外,作者使用doxycycline诱导α-Syn A53T表达的PC12α-Syn A53T细胞,验证GM1神经节苷脂对自噬和α-Syn清除的影响。共聚焦显微镜结果(图5a)显示,在PC12α-Syn A53T细胞中,GM1神经节苷脂处理后LC3斑点增加,而doxycycline诱导的α-Syn积累减少,其中LC3和α-Syn的共定位显著增强(图5a)。Western blot分析证实,GM1神经节苷脂导致α-Syn蛋白水平下降,而3-MA共处理逆转了这一趋势(图5b)。与GM1神经节苷脂类似,Rapamycin也能强烈降低α-Syn水平(图5b)。作者采用化学反应方法,用荧光FITC荧光标记GM1神经节苷脂。在受GM1-FITC处理的PC12α-Syn A53T细胞中观察到强烈的绿色荧光(图5c)。同时,在PC12α-Syn A53T细胞中,GM1-FITC和α-Syn以及GM1-FITC和LC3之间观察到明显的共定位(图5d)。综上所述,这些数据表明GM1神经节苷脂激活自噬来清除α-Syn的积累。
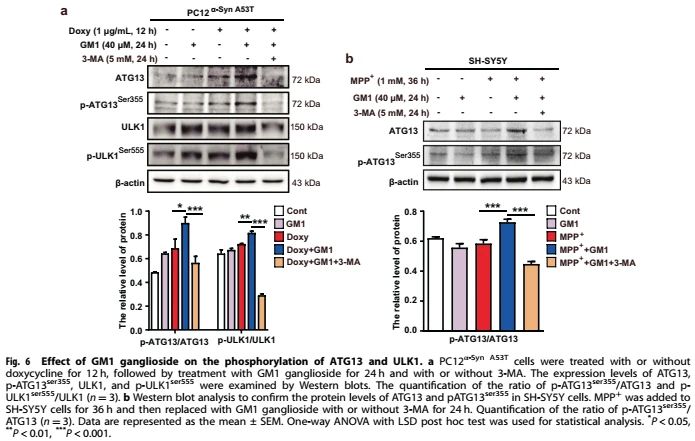
5. ATG13-ULK1复合物参与GM1神经节苷脂诱导的自噬
ULK复合体由ULK1、ATG13、FIP200和ATG101组成,它们是启动自噬过程所必需的。作者评估了GM1神经节苷脂对ULK1和ATG13蛋白表达水平的影响。值得注意的是,GM1神经节苷脂处理促进了PC12α-Syn A53T细胞中ATG13和ULK1的磷酸化(图6a)。然而,GM1神经节苷脂的作用被3-MA抑制(图6a)。同样,GM1神经节苷脂处理的SH-SY5Y细胞也显示出p-ATG13/ATG13的比例增加,而3-MA处理抑制了GM1神经节苷脂的这种作用(图6b)。综上所述,GM1神经节苷脂通过激活ATG13-ULK1复合物来诱导自噬。
总结
总的来说,作者通过MPTP/MPP+处理建立了α-Syn过表达模型,以评估GM1在体内和体外对PD的治疗作用。此外,使用表达诱导型α-Syn的PC12α-Syn A53T细胞来证明GM1和α-Syn之间的直接关系。研究结果表明,自噬的激活解释了GM1神经节苷脂的抗PD作用,并为GM1神经节苷脂清除α-Syn的机制提供了可能的理论基础。



 返回列表
返回列表